Presentazione
Criobanca di ceppi di batteri patogeni isolati da infezioni periprotesiche e chirurgiche
E' costituita una ceppoteca nella quale sono raccolti gli isolati clinici di batteri responsabili di infezioni periprotesiche e chirurgiche diagnosticate e curate negli Istituti Ortopedici Rizzoli.
I campioni batteriologici provenienti dal settore di microbiologia vengono processati con una procedura idonea a garantire l'identificazione, il controllo, la vitalità e lo stoccaggio dei ceppi microbici.
1. Consistenza della ceppoteca
Attualmente sono raccolti oltre 2.700 isolati clinici, ottenuti da pazienti sottoposti a revisione di infezioni chirurgiche e a trattamento di protesi infette nell'Istituto Ortopedico Rizzoli. I singoli ceppi sono conservati a -80°C in vial crioresistenti, sospesi in fluido di crioconservazione composto da 90% brodo nutritivo e 10% glicerolo. La coltura di ogni singolo ceppo è suddivisa e conservata in campioni multipli, dei quali parte riservati al back-up. I campioni sono progressivamente numerati e ricevono un codice tale da garantire il rispetto delle norme sulla privacy.
2. Identificazione
L'identificazione, eseguita con gallerie biochimiche API, è controllata mediante ribotipizzazione con lo strumento RiboPrinter® (DuPont). L'identificazione è attuata a livello di specie, subspecie e ribotipo.
3. Antibioticoresistenza
La sensibilità agli antibiotici è eseguita con il metodo della diffusione in agar (Kirby-Bauer) secondo le linee guida del National Committee for Clinical Laboratory Standards. Sono utilizzati dischi di 16 differenti antibiotici alle concentrazioni suggerite dal National Committee for Clinical Laboratory Standards Institute (CLSI). I diametri delle aree di inibizione della crescita sono misurati in mm mediante un sistema di analisi d'immagine dedicato (Biovideobact, Biokit), che misura automaticamente i diametri degli aloni di inibizione e consente, se necessario, di misurare la MIC dei singoli antibiotici.
4. Caratterizzazione fenotipica per la produzione di biofilm
I ceppi sono valutati per la capacità di produrre biofim. Nel caso di stafilococchi la valutazione era eseguita con il metodo di coltura in agar-rosso Congo, secondo una originale procedura ottimizzata messa a punto nel Laboratorio di Patologia delle Infezioni Associate all'Impianto e pubblicata [Biomaterials. 2002;23(21):4233-9]. Attualmente sono stati messi a punto nel nostro Laboratorio nuovi metodi per la quantificazione e la caratterizzazione delle diverse componenti macromolecolari del biofilm.
5. Caratterizzazione genotipica
I ceppi sono analizzati mediante metodi di biologia molecolare (PCR con adatti primers e DNA-ibridazione con adatte sonde) per la presenza dei geni per la produzione di polisaccaride del biofilm (geni del locus ica), dei geni delle adesine alle proteine della matrice dell'ospite (MSCRAMMs), e dei geni delle tossine.
6. Ribotipizzazione
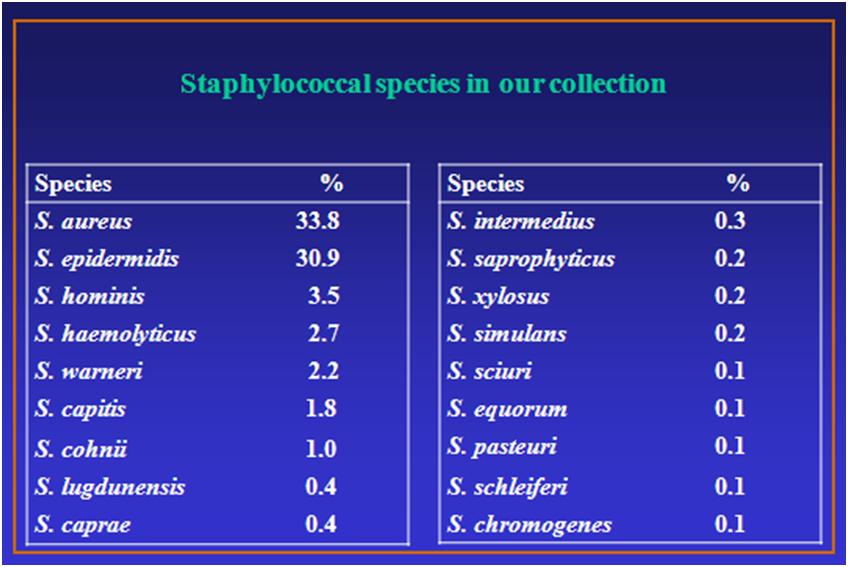
Specie batteriche isolate e conservate nella ceppoteca
L'identificazione mediante il RiboPrinter® viene eseguita in modo particolare su specie rare, solitamente batteri opportunisti, o patogeni di origine animale (S. caprae, S. equorum ed altri), definendone il ribogruppo e confrontando i dati con la banca dati della DuPont. Particolare attenzione è riservata alla collezione di specie di stafilococchi coagulasi-negativi che vanno emergendo come 'nuovi patogeni'.
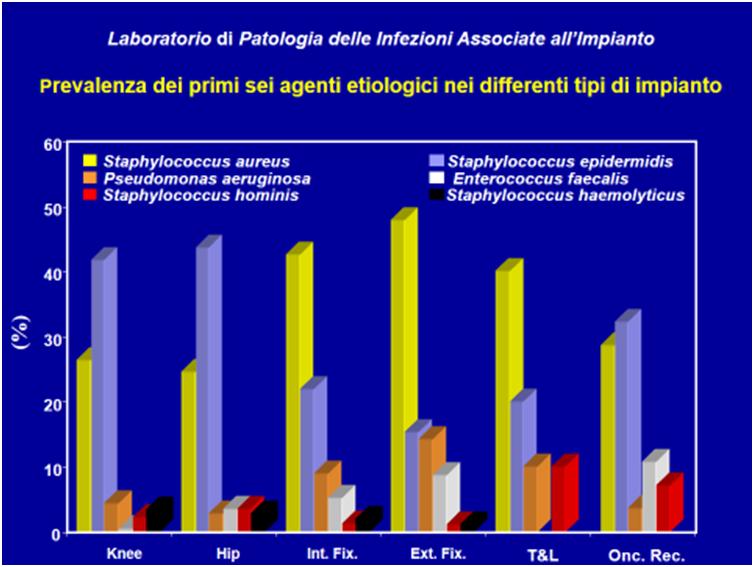
Nel caso dei principali agenti etiologici di infezioni associate agli impianti ortopedici, la ribotipizzazione è utilmente impiegata per individuare i cloni epidemici.